Teorema Ekipartisi dan Energi Dalam (U)
TEOREMA EKIPARTISI
Ada 3 jenis Gas:
1.
Gas monoatomic (Contoh: Ar dan He)
2.
Gas diatomic (Contoh: O2 dan H2)
3.
Gas poliatomik (Contoh: H2O dan CO2)
Teorema Ekipartisi:
Setiap energy yang mungkin diserap oleh gas hanya bergantung pada temperature
dan mempunyai porsi yang sama. Energy Total gas adalah jumlahan semua jenis
energy tersebut.
Persamaan energy kinetic diatas dikhususkan untuk gas
monoatomic.
Persamaan tersebut dapat kita tuliskan sebagai berikut:
Gerak Translasi.
Gerak
Rotasi
Pada gas monoatomic, pada suhu berapapun
partikel hanya akan mengalami gerak translasi pada sumbu x, y, dan z. Maka dari
itu nilai derajat kebebasan sistemanya berjumlah 3.
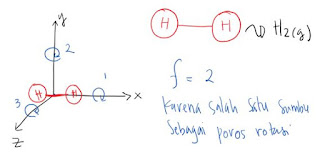
2. Pada gas diatomik
Pada gas diatomic, nilai derajat kebebasan
dipengaruhi oleh suhu.
3. Pada gas poliatomik
Biasanya diketahui di soal.
ENERGI DALAM (U)
Energi dalam berasal dari energy kinetic
partikel gas karena energy ikat yang diabaikan. Energi dalam merupakan energy
kinetic rata-rata dikalikan banyak partikel yang ada dalam ruangan.
Latihan Soal
1. 1. Gas diatomic pada suhu 47oC
memeiliki energy kinetic sebesar . . .
2. 2. Gas poliatomik pada suhu 1.200 K melakukan 4
trabslasi, 3 rotasi, dan 3 vibrasi. Jumlah zat gas sebanyak 3 mol. Energi
kinetic rata-rata dan energy dalamnya adalah . . .
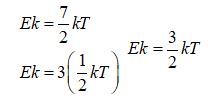







Komentar
Posting Komentar